Durchfall, Kotabsatz mit erhöhtem Wassergehalt und/oder einer erhöhten Frequenz, ist auch bei Kleinsäugern einer der häufigsten Vorstellungsgründe. Der Therapieerfolg ist abhängig vom Wissen um die tierartspezifischen Durchfallursachen und die systematische Aufarbeitung.
Durchfallursachen
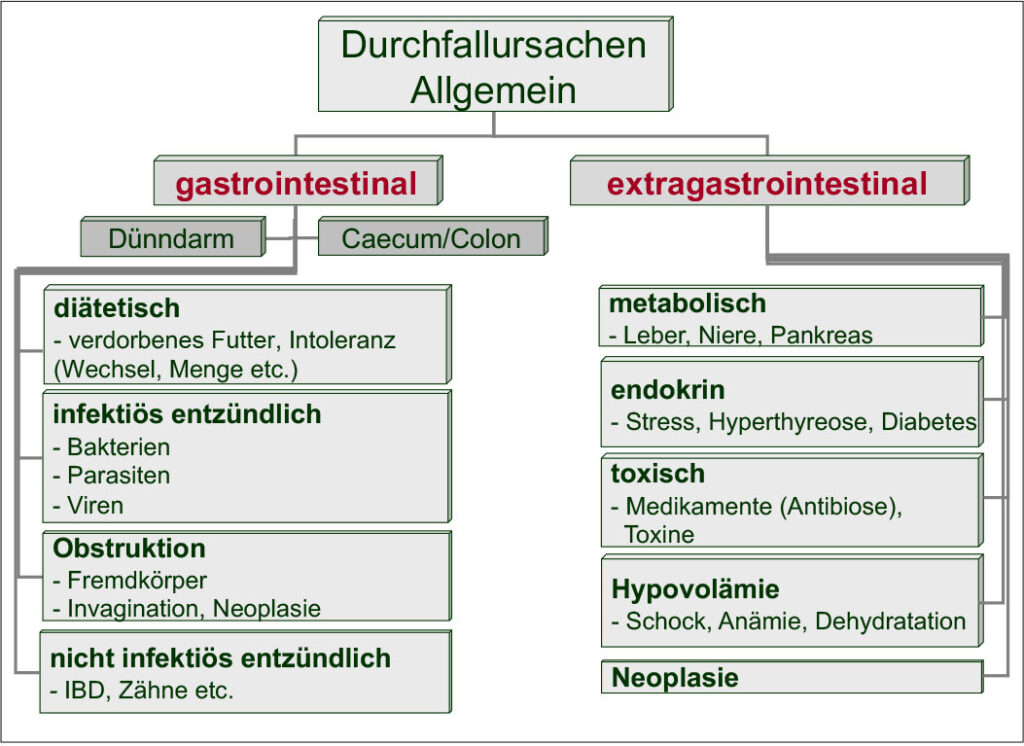
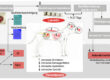
Die Durchfallursachen (Abb. 1) sind ebenso vielfältig wie die Zahl der Kleinsäugerarten und ihre Unterschiede in Anatomie, Physiologie und Krankheitsprädisposition.
Die Einteilung des Durchfalls erfolgt wie bei Kleintieren zunächst nach bestimmten Kriterien (in Anl. an Steiner, 2009):
- Dauer: akut (< 1 Woche) und chronisch (> 3 Wochen)
- Lokalisation: Dünn- und/oder Dickdarm
- Pathophysiologie: osmotisch (Intoleranz, Laktulose etc.), sekretorisch (pathogene Keime, Intoxikationen, chron. Entzündung etc.), abnorme Permeabilität (pathogene Erreger, Entzündung, Schock etc.) oder Störungen der Motilität (Obstruktion, Hyperthyreose etc.)
- allgemeine Ursachen (Abb. 1)
Durchfall oder Caecotrophe
Herbi- und granivore Kleinsäuger fressen einen Teil des bereits vorverdauten Blinddarmkotes (Coprophagie), um die Effizienz der Verdauung zu erhöhen. Bei Kaninchen ist dieser Kot (Caecotro-phe) auch optisch vom Hartkot unterscheidbar.
Physiologische Caecotrophe ist faserarm, dunkel, glänzend (Schleimschutz vor Magensäure), traubenkernförmig zusammengeballt und wird v. a. nachts intermittierend (im Wechsel mit geformtem Kot) abgesetzt und direkt vom Anus aufgenommen.
Ist die Aufnahme gestört (Wirbelsäulenprobleme, Adipositas etc.) oder nimmt die Blinddarmfüllung durch Fehlernährung (wenig Fasern, viel Kohlenhydrate) zu, verändert sich auch Menge, Farbe und Konsistenz der Caecotrophe (mehr, heller, weicher) und sie bleibt liegen. Unwissende Besitzer verwechseln sie dann oft mit Durchfall. Sie sehen dann die plattgetretene Caecotrophe als Verschmutzung an den Hinterpfoten und/oder im Anogenitalbereich.
Weicher Hartkot wird in diesen Fällen weiterhin kontinuierlich abgesetzt.
Aufarbeitung:
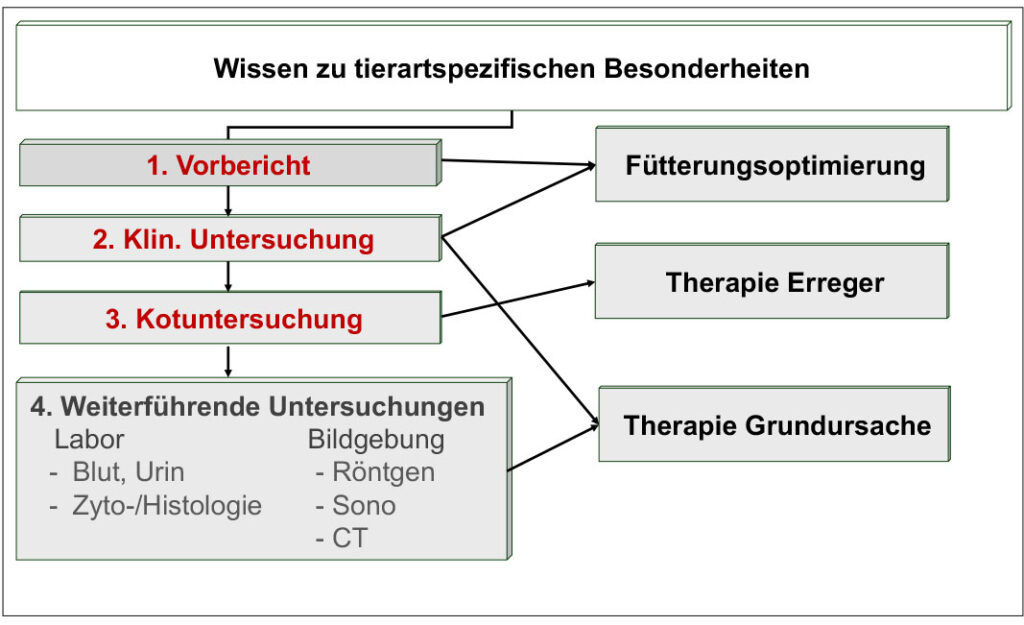
Kleinsäuger haben gern mehrere Probleme und eine alleinige Kotuntersuchung ist selten ausreichend zur erfolgreichen Therapie. Die Aufarbeitung folgt, unabhängig von der Tierart, idealerweise einem bestimmten Schema (Abb. 2). Vorbericht (seit wann, intermittierend/kontinuierlich, mögliche Ursachen (Fütterung, Stressoren, andere Probleme etc.)) und gründliche klinische Allgemeinuntersuchung liefern oft schon wichtige Hinweise auf mögliche Ursachen. Weiterführende Untersuchungen und Therapie erfolgen je nach erhobenen Befunden.
Kotuntersuchung – ein Muss:
Die Kotgewinnung ist denkbar einfach. Der Kot kann aus der Einstreu gesammelt (spezielle Kotprobenröhrchen max. ¾ füllen) oder durch Rektalabstrich (Ausstrich direkt auf Objektträger) gewonnen werden. Der Versand in das Labor erfolgt in speziellen Umverpackungsröhrchen mit saugfähiger Einlage.
-
Abb. 1: Durchfallursachen bei Kleinsäugern allgemein
Bildquelle: J. Hein
-
Abb. 2: Systematische Durchfallaufarbeitung
Bildquelle: J. Hein
-
Abb. 3: Endoparasiten des Kaninchens im Größenvergleich
Bildquelle: Laboklin (KI-generiert)
-
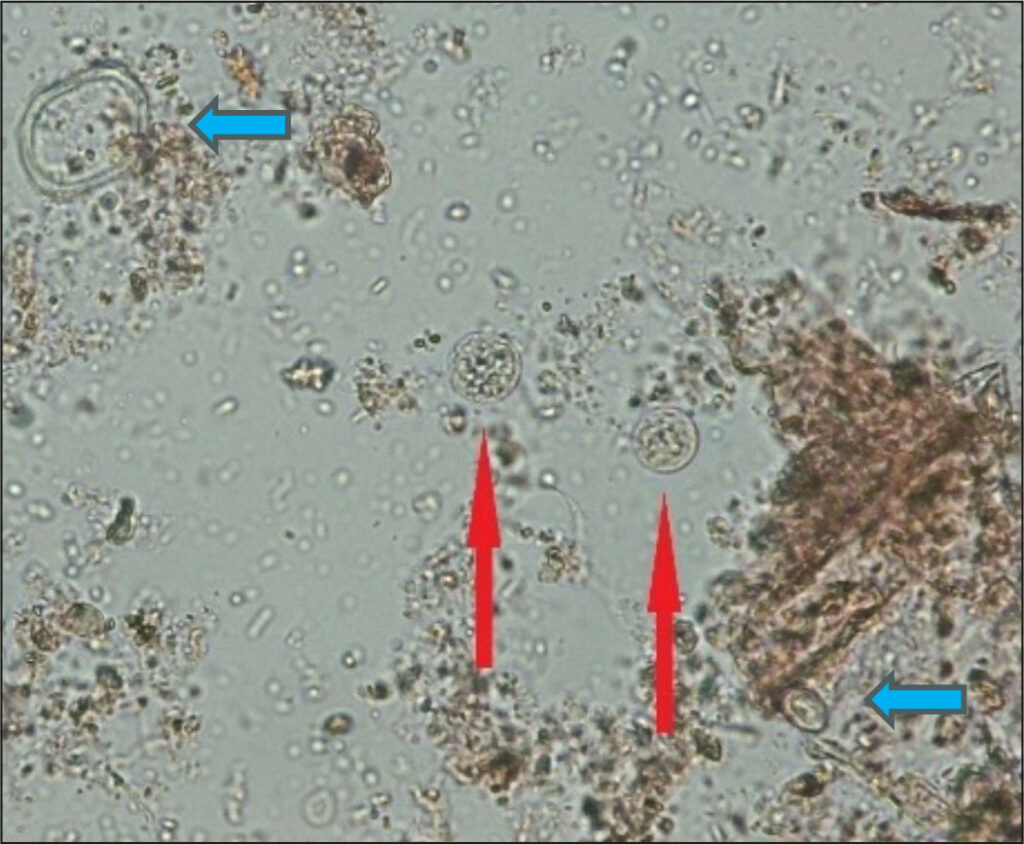
Abb. 4: Pollen (rote Pfeile) und Pflanzenrückstände (blaue Pfeile)
im Flotationspräparat, die mit Parasitenstadien verwechselt
werden können (Vergrößerung 1:400)
Bildquelle: Laboklin
-
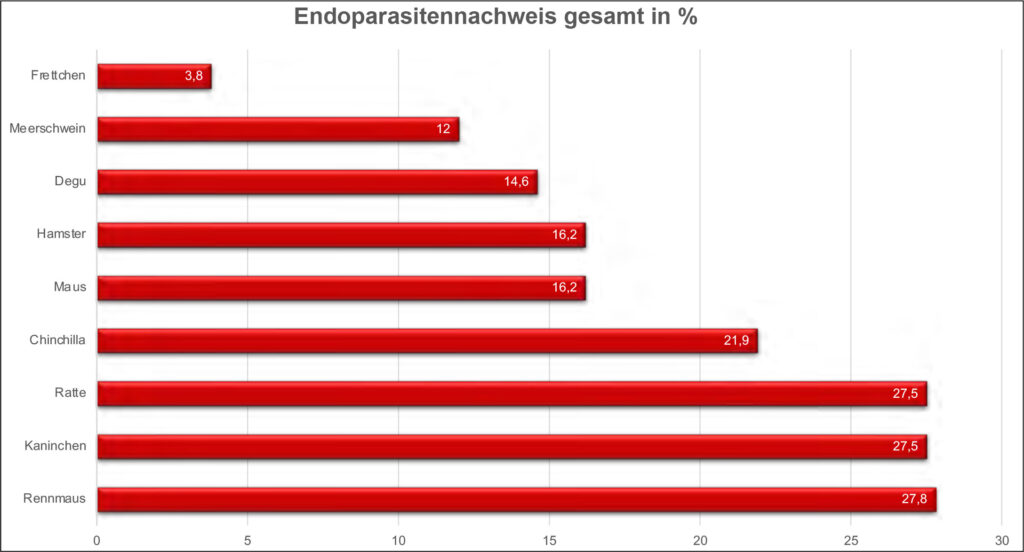
Abb. 7: Endoparasitennachweis bei verschiedenen Kleinsäugerarten in Prozent (%) (Zusammenfassung aus Csokai & Müller 2018,
Csokai et al. 2024)
Bildquelle: Laboklin
Die makroskopische und mikroskopische Kotuntersuchung gehören zu jeder Durchfallabklärung dazu („Pflicht“)!
Die makroskopische Untersuchung (Menge, Farbe, Form, Größe und Fasergehalt) lässt bereits Rückschlüsse auf Futteraufnahme (viel, wenig), Fütterung (faserarm, kohlenhydratreich), Beimengungen (Haare, Fremdkörper) und bestimmte gastrointestinale Ursachen (Megacolon, Typhlocolitis etc.) zu und kann einfach in der Praxis erfolgen.
Die mikroskopische Untersuchung erfolgt, je nach Indikation, aus Frischkot (in der Praxis) oder Sammelkot (in Praxis oder Labor). Frischkot (Rektalabstrich oder frisch abgesetzt) ist besonders für den Nachweis von beweglichen Einzellern geeignet. Diese sind nur kurz im abgesetzten Kot lebensfähig und durch die Transportzeit zum Labor dort meist nicht mehr nachzuweisen. Die Untersuchung von Sammelkot erhöht die Sensitivität der Untersuchung v. a. in Bezug auf intermittierend ausgeschiedenen Parasitenstadien und Hefen (Cyniclomyces guttulatus). Hefen sind bis zu einem gewissen Grad physiologische Bestandteile der Darmflora und gelten bei steigender Anzahl als hervorragender Indikator für Dysbiose und den Kohlenhydratgehalt in der Nahrung.
Für ein Nativpräparat reicht ein frischer Rektalabstrich mit einem Tropfen lauwarmem Wasser oder ein Tropfen einer Kotsuspension (erbsengroße Kotmenge) auf einem Objektträger mit Deckglas aus. Besteht bei Kaninchen Passalurus-Verdacht, ist es am erfolgversprechendsten mit einem Klebestreifen den Analbereich direkt zu beproben, diesen auf einem Objektträger aufzukleben und direkt unter dem Mikroskop zu untersuchen.
Sammelkot (Kot von drei Tagen) wird i. d. R. nach Anreicherung durch Flotation untersucht. Bei der Flotation werden leichte Parasitenstadien (Kokzidienoozysten, Nematodeneier etc.) in Flotationslösung mit höherer Dichte an die Oberfläche transportiert und können mit einem aufgelegten Deckgläschen abgenommen werden. Die Anreicherung kann mit kommerziell erhältlichen Testkits auch in der Praxis durchgeführt werden.
Die einfachste Art mikroskopische Kotpräparate, gerade von Kaninchen, schnell durchzuscannen, ist zunächst in der 1:100 Vergrößerung (10er Objektiv) die Ebenen einzustellen, in der die Hefen gut zu sehen sind. Hefen sind ca. 10–15 µm groß und somit die kleinsten interessanten Stadien bei der Kotuntersuchung. Kokzidienoozyten (ca. 30 µm) und v. a. Nematodeneier (ca. 100 µm) sind deutlich größer und so einfacher zu finden (Abb. 3).
Worauf geachtet werden sollte, ist, dass Pollen, andere Pflanzenbestandteile und Milbeneier nicht mit Parasitenstadien verwechselt werden (Abb. 4).
Eine andere Form der Anreicherung, das Auswanderungsverfahren (nach Baermann-Wetzel), wird zum Nachweis von Crenosoma striatum-Larven (Lungenwurmlarven) angewendet. Da schneckenfressende Igel (europäische Igel) neben anderen Endoparasiten auch häufig stark mit Lungenwürmern infiziert sind, sollte bei ihnen, zusätzlich zur Untersuchung nach Flotation (Capillaria spp.), auch immer die Kotuntersuchung mittels Auswanderung (Crenosoma striatum) angefordert werden.
Je nach Tierart und Verdacht sind weitere Kotuntersuchungsverfahren („Kür“) sinnvoll:
Giardien- (v. a. Chinchilla und Frettchen) und Cryptosporidien-Stadien (Mäuse, Ratten, Hamster) werden am effektivsten mittels ELISA detektiert. Die Sensitivität der im Labor verwendeten Enzym-Immunoassays (EIA) ist wesentlich höher als die der Praxis-Schnelltests (Nicht-Enzym-Immunoassays), die z. T. auch falsch-positive Ergebnisse liefern und somit eher als Screeningtests dienen.
Für einige Erreger, v. a. Viren (z. B. Rota-, Corona-, Aleuten-disease-Virus (ADV)), aber auch Bakterien (Salmonella spp., Lawsonia intercellularis) und einige Protozoen (z. B. Cryptosporidien-Differenzierung) werden auch PCR-Tests angeboten. Die PCR gilt als sehr sensitiv, ist aber wegen der intermittierenden Ausscheidung der Erreger auch nur positiv beweisend.
Die zusätzliche bakteriologische Untersuchung (BU) ist immer sinnvoll bei Kleinsäugern mit weniger Darmflora (Carnivora, Insectivora, Granivora). Bei Herbivoren mit ausgeprägter, physiologischer Darmflora (alles kann vorkommen) ist sie häufig wenig aussagekräftig, außer es werden gezielt humanpathogene Bakterien (Salmonellen etc.) oder spezielle Erreger, wie Klebsiellen (V. a. Typhlocolitis), gesucht.
Die mykologische Untersuchung (MU) muss selten separat durchgeführt werden, da Hefen (Gradmesser der Dysbiose, selten primäres Pathogen) bereits im Nativ- oder Flotationspräparat sichtbar sind. Gerade beim Hamster sollte aber ggf. auch an Candida spp. als Durchfallauslöser gedacht werden. Diese sind mikroskopisch nicht identifizierbar und müssen mittels Kultur angezüchtet werden.
Heutzutage erfolgt der Virusnachweis im Kot mit erregerspezifischen PCRs. Im Gegensatz zu der früher verwendeten Elektronenmikroskopie, bei der alle vorhandenen Viren detektierbar waren, muss heutzutage gezielt auf einzelne Viren getestet werden. Dies erklärt, warum Virusenteritiden zwar weiterhin vorkommen, jedoch unterdiagnostiziert sind.
Welche Kotuntersuchung bei welchen Kleinsäugern sinnvoll/wichtig sind, ist in Tab. 1 für Sie aufgelistet.
Tab. 1: Sinnvolle Kotuntersuchungen bei verschiedenen Kleinsäugern (rot/fett = „Pflichtuntersuchungen“)
| Gruppe | Herbivore | Granivore | Carnivore | Insectivore | |||
| Tierart | Kaninchen | Meerschwein | Chinchilla, Degu | Maus, Ratte, Rennmaus | Hamster | Frettchen | Igel |
| Haupterreger | Eimeria, Passalurus | Protozoen | Giardien | Oxyuren | Oxyuren | Eimeria, Giardien | Nematoden |
| Untersuchungsverfahren | |||||||
| Makroskopie | X Caecotrophe? |
X | X | X | X | X | X |
| Mikroskopie | |||||||
| – nativ (frisch) | X | X | X | X | X | X | X |
| – Flotation | X | X | X | X | X | X | X |
| – Auswanderung | X Schneckenfresser | ||||||
| ELISA | |||||||
| – Giardien | X | (X) | (X) | X | |||
| – Cryptosporidien | X (Futtertiere) |
||||||
| BU/MU | spez. Verdacht | ? | (X) | (X) Candida | X | X | |
| PCR | Rotaviren, Salmonellen | Differenzierung, Cryptosporidien | Lawsonia | Coronaviren, ADV | |||
Darmparasiten – wie häufig sind sie wirklich?
Aktuelle Auswertungen von eingesandten Kotproben (Csokai & Müller 2018, Csokai et al. 2024) zeigen, dass Endoparasiten in nur 4–28 % mikroskopisch (nach Flotation) detektiert wurden. Die meisten Endoparasiten-positiven Proben waren bei Rennmäusen (27,8 %), Ratten (27,5 %), Kaninchen (27,5 %) und Chinchilla (21,9 %) zu finden; bei Frettchen waren es nur 3,8 % (Abb. 7).
Zu den häufigsten Erregern zählten die Protozoen mit Giardia spp. (Chinchilla 21,9 %, Ratte 13,1 %, Degu 10,7 %), Eimeria spp. (Kaninchen 20,6 %, Meerschweinchen 3,5 %) und Oxyuren (Gerbil 21,1 %, Maus 13,2 %, Hamster 9,4 %). Da es sich i. d. R. um Sammelkotproben handelt und die Nachweishäufigkeit v. a. von beweglichen Einzellern mikroskopisch mit der Zeit stark nachlässt, ist die Frage wie viele Proben auf diese Parasitenpopulation bezogen falsch-negativ getestet werden.
Merke: Die meisten Durchfälle bei Kleinsäugern sind nicht endoparasitär bedingt!
Diätische Ursachen und nachfolgende Dysbiosen sind wesentlich häufiger.
Fazit:
Wissen zu tierartspezifischen Besonderheiten und Krankheitsprädispositionen ist Voraussetzung für eine erfolgreiche Durchfallaufarbeitung. Die Kotuntersuchung ist wichtig und gehört zur Abklärung dazu – das Gesamtbild aber auch! Denn ist die Kotuntersuchung negativ und die Fütterungsoptimierung nicht ausreichend, helfen andere weiterführende Untersuchungen bei der Ursachenfindung.
Dr. Jutta Hein, Dr. Britta Beck
| Unsere Leistungen zum Thema im Überblick | |
| Einzelverfahren | |
| # 149 | Parasitologische Untersuchung (Flotation, SAFC) |
| # 585 | Auswanderungsverfahren (Lungenwurmlarven) |
| # 187 | Cryptosporidien-Antigen (EIA) |
| # 185 | Giardia sp.-Antigen (EIA) |
| Kotprofile | |
| # 2170 | Kotprofil Kaninchen und Nager (Bakteriologie inkl. Salmonellen, Mykologie inkl. Cyniclomyces guttulatus, Endoparasiten) |
| # 1177 | Kotprofil Frettchen (Bakteriologie inkl. Salmonellen, Mykologie, Endoparasiten, Giardia sp.-Antigen (EIA)) |
| # 87 | Parasitenprofil Frettchen und Chinchilla (Endoparasiten, Giardia sp.-Antigen (EIA)) |
| # 89 | Parasitenprofil Igel (Endoparasiten, Auswanderungsverfahren (Lungenwurmlarven)) |