Die glomeruläre Filtrationsrate (GFR) reflektiert als Basisfunktion der Niere frühzeitig und am deutlichsten eine Funktionseinschränkung des Organs. Insbesondere bei der Katze ist es notwendig die GFR zu ermitteln, da sie meist erst spät einen Verlust des Konzentrationsvermögens des Harnes zeigt. Eine Schädigung der Glomeruli kann zum anderen einen Barriereverlust für Proteine bedeuten, sodass diese vermehrt mit dem Harn ausgeschieden werden (Proteinurie).
Die GFR gibt das Gesamtvolumen des Primärharns an, das von allen Glomeruli beider Nieren zusammen in einer definierten Zeiteinheit gefiltert wird. Diese sinkt pathologisch bei Nierenerkrankungen verschiedenster Art. Im Routinelabor wird zur Abschätzung der GFR die Untersuchung auf Kreatinin und Cystatin C im Serum durchgeführt. Bei einer reduzierten GFR kommt es zu einem Anstieg der genannten Parameter im Serum. Die modifizierte Plasma-Clearance von exogenem Kreatinin zeigt sich in der Praxis als praktikabler Funktionstest der Niere.
Kreatinin ist ein physiologisches Endprodukt des Muskelstoffwechsels. Ein annähernd konstanter Teil des Kreatins (Vorstufe des Kreatinins) wird laufend umgewandelt, der Kreatininspiegel wird somit vor allem durch die Muskelmasse bestimmt. Die Konzentration im Serum ist weitgehend von Stoffwechsellage und Diät unabhängig. Durch Muskelfleisch in der Nahrung kann eine Zunahme bis 10% hervorgerufen werden. In der Niere wird Kreatinin vollständig glomerulär filtriert, tubulär findet bei Hund und Katze nur eine untergeordnete Rückresorption statt. Daraus ergibt sich, dass Kreatinin eine geeignete Messgröße der glomerulären Filtration ist. Kreatinin weißt eine hohe Spezifität auf, jedoch können erhöhte Werte erst gemessen werden, wenn 3/4 der Nierenfunktion ausgefallen ist. Bei muskelarmen Tieren (z.B.: auszehrenden Allgemeinerkrankungen, Muskelerkrankungen) können trotz verminderter GFR Kreatininwerte im Normalbereich bestimmt werden. In solchen Fällen kann ein erhöhtes Cystatin C dieser Patienten als diagnostische Hilfestellung dienen.
Cystatin C ist ein sehr kleines Protein (Cystein-Proteasen-Inhibitor). Es wird in nahezu allen kernhaltigen Körperzellen relativ konstant gebildet. Die Produktion wird nur durch wenige extrarenale Faktoren beeinflusst. Bei Tieren mit manifester Hyperthyreose oder durch hochdosierter Glukokortikoidgabe kann der Cystatin C Wert im Serum erhöht sein. Eine Reduktion der Bildungsrate durch konsumierende Erkrankungen findet nicht statt. Cave: Postprandial kann Cystatin C stark abfallen und bis zu neun Stunden erniedrigt bleiben.
Cystatin C wird in den Glomeruli vollständig filtriert. Beim Menschen wird es zur Nierenfunktionsdiagnostik im „Kreatinin-blinden“ Bereich eingesetzt, da schon bei moderaten Einschränkungen der GFR erhöhte Werte messbar sind.
Untersuchungen bei Hunden mit einer renalen Malfunktion im subklinischen „Kreatinin-blinden“ Bereich (40%<GFR<100%) haben für Cystatin C und Kreatinin ähnlich gute diagnostische Qualität ausgestellt (Hartmann 2007). Eine neuere Studie von Wehner 2008 zeigt für Cystatin C eine bessere Korrelation mit der GFR und eine höhere Sensitivität als für Serum-Kreatinin. Bei der Katze gibt es derzeit keine Studien, die den Wert des Cystatins belegen. Mehrmalige Messungen von Cystatin C (im Rahmen von geriatrischen Vorsorgeuntersuchungen) können nach unseren Beobachtungen eine beginnende Problematik darstellen.
Für eine zuverlässige Abklärung von verdächtigen Fällen ist die Bestimmung der GFR über eine Clearance Messung zu empfehlen. Die Indikationen sind der Verdacht auf renale Malfunktion bei nicht azotämischen Tieren, grenzwertige bzw. leicht erhöhte Kreatininwerte, eine morphologisch veränderte Niere, Rassedisposition und Vorsorgeuntersuchung älterer Patienten. Bei existierender Malfunktion oder bei akutem Nierenversagen kann mit der Clearance das Ausmaß des Schadens bestimmt werden. Die Ergebnisse können zur Prognoseeinschätzung, Therapiekontrolle und Korrektur von Dosierungen nierengängiger Medikamente genutzt werden.
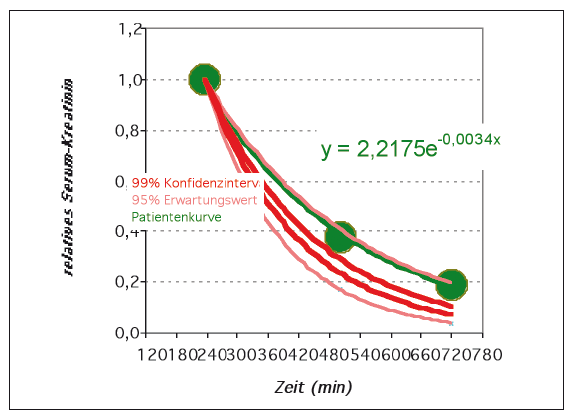
- Abb. 1: relative terminale Kreatinin-Clearance bei einer Katze
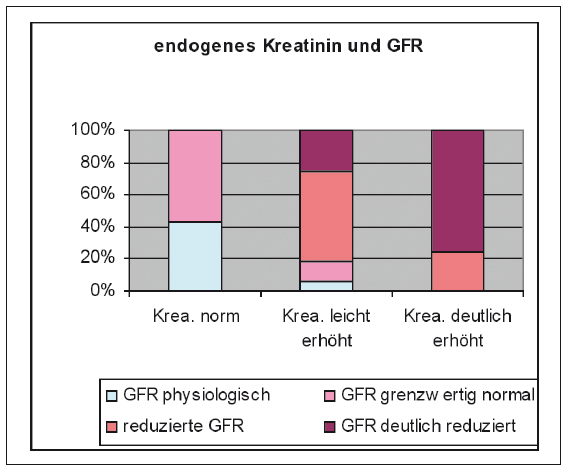
- Abb. 2: relative Verteilung von endogenen Kreatinin und GFR bei 25 Hunden
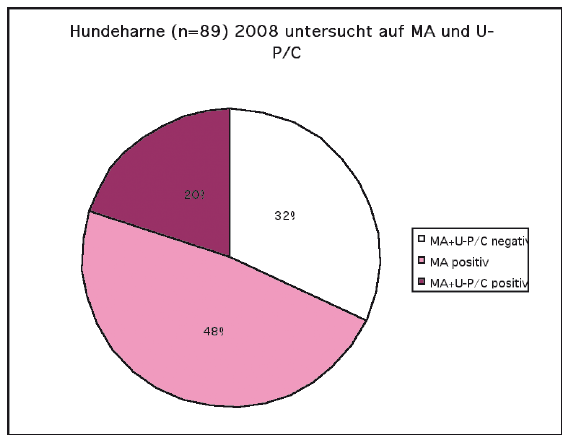
- Abb. 3: relative Verteilung von Mikroalbumin und U-P/C positiven Harnen von Hunden
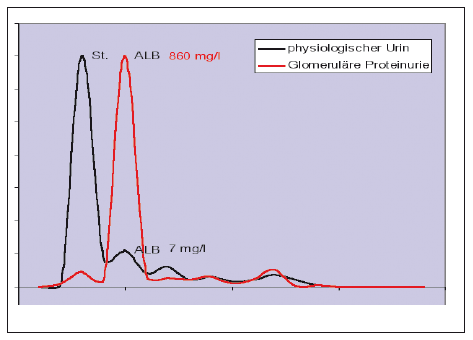
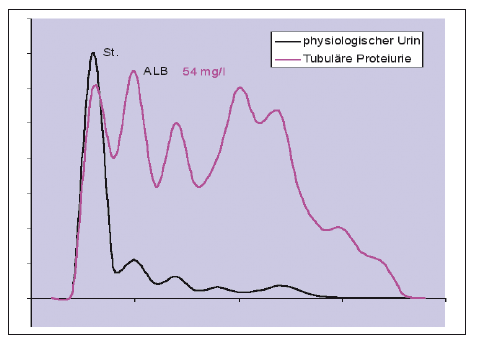
- Abb. 4: Harnelektrophorese mit relativer Darstellung des Albuminverlusts
- Abb. 5: Harnelektrophorese mit relativer Darstellung der tubulärer Proteinurie
Bei LABOKLIN testen wir die modifizierte Plasma-Clearance von exogenem Kreatinin.
Damit überprüft man die Filtrationsleistung der Niere mittels Messung der Ausscheidungsgeschwindigkeit von exogenem Kreatinin als Markersubstanz. Abhängig von der Körperoberfläche (KOF) des Tieres (Umrechnungstabelle: kg KGW in m2 KOF) wird eine genaue Menge der 5%igen Kreatininlösung verabreicht, nachdem die Serumprobe für den Ausgangswert (= Probe 0) entnommen wurde. Kreatinin verteilt sich unabhängig von der Verabreichungsform (i.v., s.c) sehr rasch im Körper, zeitgleich setzt bereits die renale Ausscheidung ein. Im Zeitfenster von 3 bis 8 Stunden nach der Kreatininapplikation wird die Blutabnahme für die Proben 1, 2 und 3 im Mindestabstand von einer Stunde durchgeführt. Zwei der Werte sind für die Berechung der GFR ausreichend, der dritte sichert die Richtigkeit der Testdurchführung ab. Wichtig ist die minutengenaue Zeitangabe der Probennahme, die einfach durch Einschalten einer Stoppuhr zu Beginn (=Kreatininapplikation) ermittelt werden kann. Eine Verschlechterung der Niereninsuffizienz durch die Durchführung des Funktionstest ist nicht zu erwarten, da der erhöhte Kreatininspiegel nur kurz anhält und keine echte Mehrbelastung für die Niere entsteht. Die gewonnenen Ergebnisse werden rechnerisch und grafisch ausgewertet und interpretiert. Abbildung 1 zeigt ein Beispiel der relativen terminalen Ausscheidung einer Katze. Die terminale Kreatinin-Clearance liegt für dieses Tier mit 75.7 ml/min/mÇ KOF innerhalb des Referenzbereiches (50-90 ml/min/mÇ bei der Katze). Daraus leitet sich eine GFR von 62-73 % der Norm ab (GFR ab >70% der Norm gilt als normal. Die grüne Patientenkurve ist gerade noch innerhalb des 95 %-Konfidenzintervalls). Die mit diesem Funktionstest ermittelte grenzwertig normale glomeruläre Filtrationsrate kann bereits ein Hinweis auf eine frühe beginnende Insuffizienz sein kann.
Die Proteinurie ist ein Leitsymptom fast aller Nierenerkrankungen, diese kann zur Diagnostik sehr vielfältig genutzt werden. Die Proteinurie kann als transient (Fieber, starke körperliche Anstrengung) eingestuft werden oder als pathologischer nicht transienter Eiweißverlust, welcher prärenalen, renalen oder auch postrenalen Ursprungs sein kann.
Bei 25 von LABOKLIN untersuchten Hunden, zeigt sich sehr anschaulich, dass bei leicht erhöhten Kreatininwerten (106-144µmol/l) die Filtrationsleistung der Niere in den meisten Fällen beeinträchtig ist. Die Malfunktion verschlechtert sich erwartungsgemäß mit der Zunahme des endogenen Serum-Kreatinins.
Postrenale Ursachen wie Entzündungen und Blutungen im Harntrakt sind häufige Ursachen für eine Proteinurie und sollten mittels Harnsediment und Kultur erfasst (bzw. behandelt) werden.
Prärenaler- und renaler Eiweißverlust kann über die Bestimmung des U-P/C – Quotienten quantifiziert werden. Eine genauere Klassifizierung der Proteine gelingt mit der Harnelektrophorese.
Der erste und einfache diagnostische Test ist schnell und in der Praxis durchführbar:
Der Harnteststreifen reagiert empfindlich vor allem auf Albumine und erfasst Globuline weniger verlässlich. Für eine positive Reaktion am Teststreifen muss die Albuminkonzentration im Harn 30 mg/dl überschreiten. Da die Färbung am Teststreifen jedoch pH-Wert-abhängig ist, kann es bei alkalischen Harnen zu falsch positiven Befunden kommen.
Eine Albuminkonzentration größer als normal und unter dieser Schwelle wird als Mikroalbuminurie (1 – 30mg/dl) definiert. Beim Hund und Katze steht seit geraumer Zeit die Untersuchung auf Mikroalbumin (MA) im Harn zur Verfügung. Mikroalbumin gilt als sehr sensitiver Früherkennungsmarker der glomerulären Schädigung und Einschränkung der tubulären Rückresorption. Eine Studie von 38 Rüden mit einer genetisch determinierten glomerulären Schädigung hat gezeigt, dass Mikroalbumin bis zu 16 Wochen früher als der Urin-Protein/- Kreatinin-Quotient positiv getestet werden kann. Die von Laboklin 2008 untersuchten Harne von Hunden mit erhöhtem MA (n=54) zeigen in 1/3 der Fälle einen erhöhten Urin-Protein/-Kreatinin- Quotienten (n=22).
MA eignet sich jedoch wegen einer geringen Spezifität nicht gut als Screeningparameter, wie Studien an gesunden Tieren zeigen. Wie auch in der Humanmedizin bekannt („marschinduzierte“ MA), kann es durch körperliche Belastung zu erhöhten Albuminwerten im Harn kommen. Die Testung auf MA sollte deshalb auf die folgenden Indikationen beschränkt werden, sodass aus der gewonnenen Information Therapie und Prognose verändert werden kann.
Bei Diagnosen wie Diabetes mellitus, Hypertension, Hyperthyroidismus, Neoplasien, aber auch bei chronischen Entzündungen und Infektionen (Stomatititen, Dirofilaria immitis-Infektionen, Ehrlichiose, Leishmaniose, Borreliose,…) ist die Überprüfung der MA eine sinnvolle Möglichkeit frühzeitig Nierenschäden zu erkennen.
Der Urin-Protein/-Kreatinin (U-P/C)-Quotient dient zur Quantifizierung der Proteinurie. Da beim Tier eine 24-Stunden-Urinproteinbestimmung im Gegensatz zum Menschen nicht praxisgerecht durchführbar ist, wird der U-P/C-Quotient bestimmt. Die Kreatininexkretion ist annähernd konstant, sodass eine ähnlich zuverlässige Information über den Quotienten erstellt werden kann.
Die Harnelektrophorese vermittelt einen qualitativen Überblick über die ausgeschiedenen Proteine. Durch die Ermittlung der Zusammensetzung der Proteine kann die Pathogenese der vorliegenden Proteinurie erfasst werden. Prognose und Therapie können somit präzisiert werden. Bei verändertem Proteinmuster besteht eine sehr sichere Aussage, da die Elektrophorese eine hohe Spezifität aufweist und kaum falsch positive Befunde liefert. Eine quantitative Beurteilung des Stadiums der Erkrankung wird jedoch schwierig. Weiterhin schließen normale Muster eine Störung der glomerulären Filtrationsrate nicht aus.
Bei der selektiven glomerulären Proteinurie kommt es zu einem reinen Albuminverlust. Die Basalmembran des Glomerulums stellt sich als elektrisches Maschengitter dar. Albumin wäre auf Grund der Größe (ca. 67kDa) frei filtrierbar, ist aber stark negativ geladen. Diese Barriere wird durch Hyperglykämie, Hypertonie und Endothelschäden aufgehoben. Ein selektiver Albuminverlust kann z.B. im Frühstadium einer hypertensiven und diabetischen Nephropathie oder auch bei Autoimmunerkrankungen mit Nierenbeteiligung im Anfangsstadium auftreten.
Werden zusätzlich zum Albumin auch IgG und Mikroglobuline im Urin nachgewiesen spricht man von einer unselektiven glomerulären Proteinurie. Sie kann als Hinweis auf einen progedienten Verlauf gedeutet werden. Ursachen sind u.a. eine akute Glomerulitis, systemischen Lupus und fortgeschrittene hypertensive und diabetische Nephropathien.
Familiär gehäuftes Auftreten von Glomerulopathie ist beim Dobermann Pinscher, Samoyede, Rottweiler, Greyhound, Soft Coated Wheaten Terrier, Bullterrier und Berner Sennenhund bekannt.
Die Familiäre Nephropathie beim Englischen Cocker Spaniel ist eine der erblich bedingten Erkrankungen, bei welcher ein Gentest verfügbar ist. Diese progressive Erkrankung ist durch einen Collagen Typ IV Defekt verursacht (Struktur der Basalmembran der Glomeruli) und wird autosomal-rezessiv vererbt. Klinische Zeichen treten erstmals ab dem 6. Lebensmonat oder im zweiten Lebensjahr auf.
Eine tubuläre Proteinurie entsteht durch eine verminderte Rückresorption niedermolekulärer Proteine (α-1-Mikroglobuline, Cystatin…), welche von der Trockenchemie nicht erfasst werden.
Ursachen hierfür sind die interstitielle Nephritis, Pyelonephritis, Analgetika-Nephropathien und tubulotoxische Nephropathien.
Erbliche Ursache für einen tubulären Eiweißverlust ist z.B. das Fanconi-Syndrom, eine zentrale Regulationstörung des Calcium-Phospat-Stoffwechsels. Die entstehende Hypercalcämie verursacht eine Nephrocalcinose.
Das Bild einer tubulären Proteinurie kann auch bei ungestörter, aber unzureichender Rückresorption auftreten. Überschreitet das Plasmaprotein einen Wert von über 90g/l führt dies durch Überlastung der tubulären Rückresorption zur Proteinurie (Hyperglobinurinämie bei chron. Entzündung: z.B. FIP, Ehrlichiose, Leishmaniose…).
03 / 2009