Generelles
Die Parameter, die wir für die Nierenfunktionsdiagnostik nutzen, sind so genannte Biomarker. Funktioniert die Niere nicht wie sie soll, bleiben sie im Blut zurück. Aus der Konzentration schließen wir, wie schwer die Nierenfunktionsstörung ist. Klingt einfach, ist es eigentlich auch.
Azotämie: Die Erhöhung von harnpflichtigen Substanzen im Blut nennt man Azotämie. Die klassischen Biomarker sind Harnstoff und Kreatinin.
Das Auftreten einer Azotämie bedeutet aber nicht automatisch, dass die Niere erkrankt ist. Erst wenn wir uns sicher sind, dass weder eine prärenale noch eine postrenale Azotämie vorliegt, können wir von einer Nierenerkrankung sprechen.
Urämie: Urämie ist ein Begriff für die klinischen Folgen der Nierenfunktionsstörung, die aus der Retention von toxischen Stoffwechselprodukten, Dysregulation von Wasser- und Elektrolythaushalt sowie Hormonimbalancen entstehen. Zu den Symptomen, die mit einer Urämie einhergehen, gehören u. a. Lethargie, Schwäche, Dehydratation, Inappetenz, Vomitus und Gewichtsverlust.
Azotämie und Urämie sind somit nicht dasselbe. Die renale Azotämie zeigt die Nierenfunktionsstörung an. Urämie bedeutet, dass der Patient dadurch in seiner Lebensqualität beeinflusst wird. Somit ist Ersteres wichtig für die Diagnose der Nierenerkrankung, Letzteres für die Beurteilung des klinisch relevanten Schweregrades der Erkrankung. Der Unterschied zwischen Azotämie und Urämie erklärt unter anderem, warum einige Patienten mit chronischer Nierenerkrankung (CNE) bei hohen Nierenwerten noch ein relativ gutes Allgemeinbefinden zeigen, während es anderen mit niedrigeren Werten schon schlechter geht. Die klassischen Biomarker sind zwar Indikatoren für den Grad der Nierenfunktionsstörung, zeigen aber nicht unbedingt an, welche Auswirkungen dies auf den individuellen Patienten hat. Für die meisten urämischen Toxine, die unseren Patienten das Leben schwer machen, gibt es keine kommerziell zur Verfügung stehenden Testverfahren. Eine Ausnahme bildet Indoxylsulfat (siehe weiter unten).
-
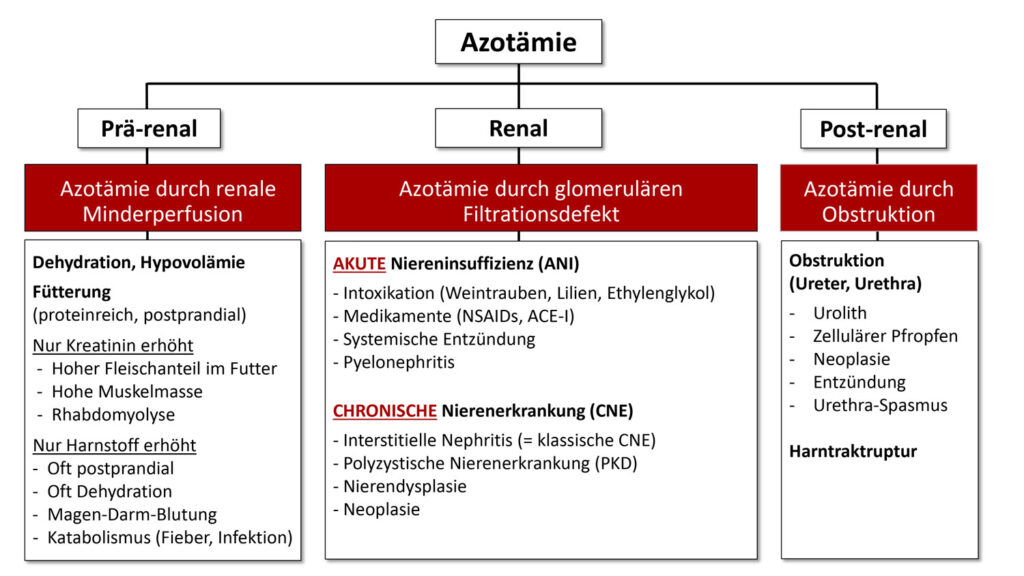
Abb. 1: Differentialdiagnosen Azotämie
Bildquelle: Dr. Jennifer von Luckner
-
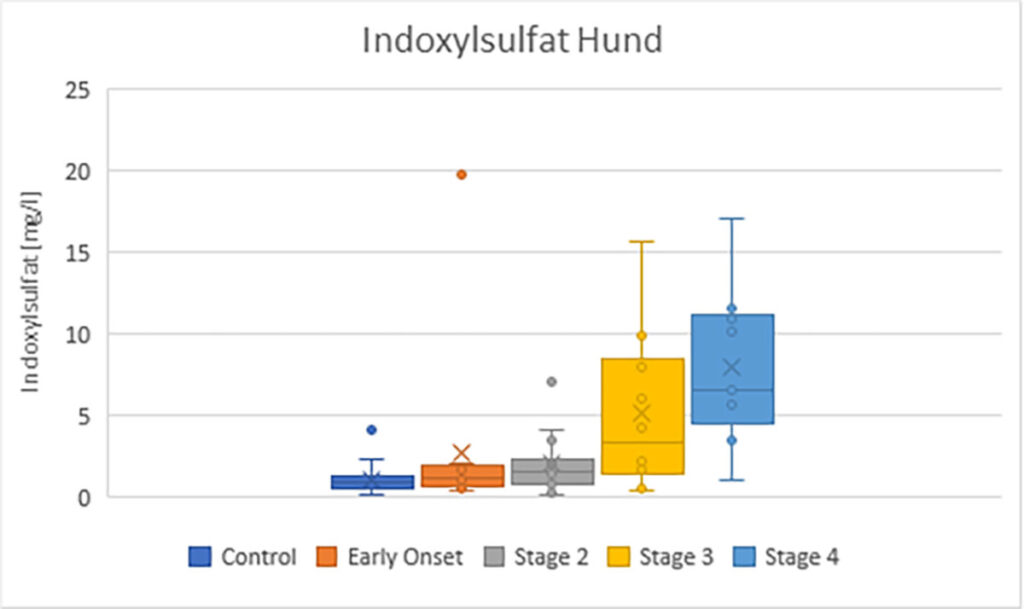
Abb. 2a: Indoxylsulfat-Konzentrationen bei Hunden mit CNE, abhängig vom IRIS-Stadium
Quelle: Laboklin, unveröffentlichte Erhebungen
-
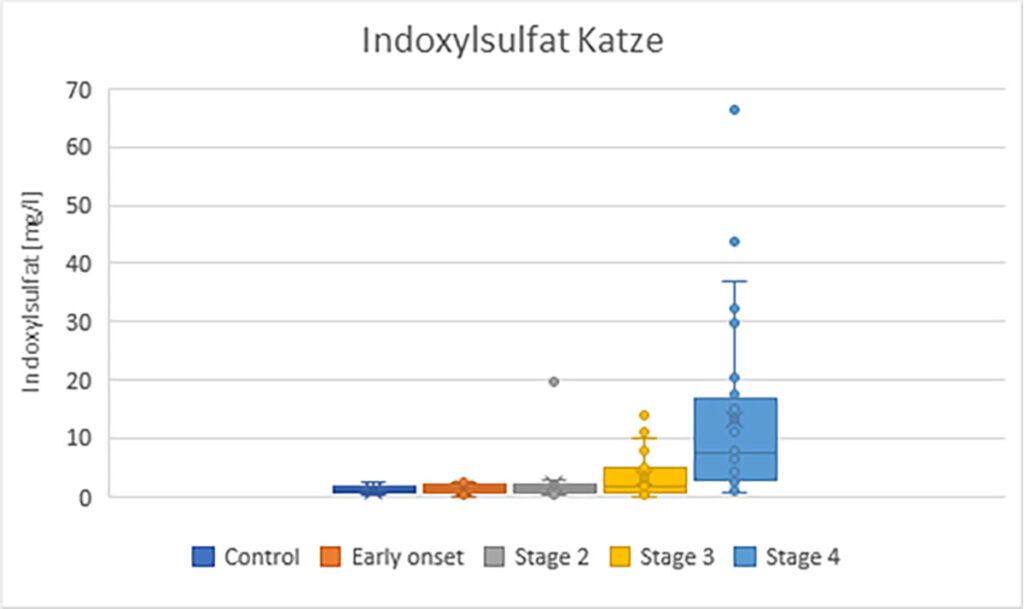
Abb. 2b: Indoxylsulfat-Konzentrationen bei Katzen mit CNE, abhängig vom IRIS-Stadium
Quelle: Laboklin, unveröffentlichte Erhebungen
In der Niere wird das zu reinigende Blut durch das Glomerulum geleitet. Dort wird das Ultrafiltrat abgepresst (glomeruläre Filtration). Dieses Ultrafiltrat wird im Tubulus nachbearbeitet. Dort werden die Stoffe, die der Körper nicht verlieren möchte (z. B. Wasser, Proteine, Glukose, Elektrolyte) zurückresorbiert.
Die im klassischen Nierenprofil überprüften Biomarker (insbesondere Kreatinin und SDMA) spiegeln überwiegend die glomeruläre Filtrationsrate (GFR) wider. Die reduzierte GFR ist aber nicht alles, was eine Nierenfunktionsstörung definiert. Die Prozesse im Tubulus spielen eine wesentliche Rolle. Sie sind es, die bei Tieren mit Nierenerkrankung zu klassischen Problemen wie Polyurie/Polydipsie, Dehydratation und Elektrolytstörungen führen.
Zudem werden viele urämische Toxine nicht nur durch die glomeruläre Filtration in den Harn ausgeschieden, sondern müssen zusätzlich – oder z. T. sogar hauptsächlich – über den Tubulus sezerniert werden. Insbesondere in fortgeschrittenen Stadien der interstitiellen Nephritis, der häufigsten Ursache chronischer Nierenerkrankungen bei Hund und Katze, wird die Tubulusfunktion zunehmend schlechter und damit für uns klinisch relevanter.
Die Biomarker der Nierenfunktionsdiagnostik
Harnstoff
Harnstoff ist ein Abfallprodukt des Proteinstoffwechsels. Er wird frei über das Glomerulum filtriert, aber partiell im Tubulus wieder rückresorbiert. Dadurch ist Harnstoff kein reiner Marker der GFR. Bei Diurese sinkt Harnstoff im Blut infolge einer reduzierten Rückresorption. Bei Dehydratation oder anderer Perfusionsstörung steigt seine Konzentration deutlicher an als die der anderen Nierenparameter. Hinzu kommt, dass der Gehalt an Harnstoff im Blut wesentlich von der Menge des mit der Nahrung aufgenommenen Proteins beeinflusst wird (Anstieg bei proteinreicher Fütterung, Abfall bei inappetentem Tier). Auch Magen-Darm-Blutungen führen zu erhöhten Harnstoffkonzentrationen. Das macht Harnstoff zu einem relativ schwierigen Parameter, wenn es um die Beurteilung der GFR geht. Aber Harnstoff hat einen Vorteil: Auch wenn er selbst nicht toxisch ist, korreliert ein erhöhter Gehalt oft gut mit einer Urämie.
Harnstoff wird optimalerweise aus Serum bestimmt. Das Blut sollte abzentrifugiert und abpipettiert werden. Ansonsten kann es durch die während des Transportes mögliche Hämolyse zu falsch hohen Messergebnissen kommen. Neben der Hämolyse kann auch eine Hyperbilirubinämie zu erhöhten Harnstoffkonzentrationen führen. Lipämisches Blut kann den Messwert reduzieren. Verwirrung stiften oft die Begriffe UREA und BUN (Blood Urea Nitrogen). Diese Parameter sind nicht vollständig gleichwertig. Nur Harnstoff (UREA) wird direkt gemessen. BUN wird über ein indirektes Messverfahren bestimmt, bei dem nicht das gesamte Harnstoffmolekül erfasst wird, sondern lediglich der darin enthaltene Stickstoff (Nitrogen). Dies ist vor allem bei Inhouse-Geräten der Fall. Möchte man beide Werte (UREA und BUN) vergleichen, müssen Korrekturformeln angewandt werden.
Kreatinin
Kreatinin entsteht vorrangig aus dem Muskelstoffwechsel und ist damit von der Muskelmasse abhängig. Es wird über das Glomerulum filtriert, aber nicht im Tubulus rückresorbiert. Damit korreliert es sehr gut mit der GFR. Entgegen der weitverbreiteten Meinung beginnt die Kreatininkonzentration bei Nierenerkrankungen schon relativ früh anzusteigen, aber erst bei einer Reduktion der GFR um 70 – 85 % steigt Kreatinin über den Referenzbereich (= Kreatinin-blinder Bereich). Es macht Sinn, sich den Wert im Nierenprofil genauer anzusehen. Ist er höher als für den Patienten zu erwarten (z. B. bei einem Patienten mit geringer Muskelmasse) oder steigt er über die Zeit an, kann das ein erster Hinweis für eine Nierenfunktionsstörung sein.
Auch wenn Kreatinin grundsätzlich ein guter Parameter zur Beurteilung der GFR ist, sollte man sich bewusst sein, dass er nicht immer entsprechend dem Grad der Nierenerkrankung erhöht ist. Bei alten Tieren mit geringer Muskelmasse sowie bei Hyperfiltration durch systemische Hypertension oder bei Hyperthyreose kann Kreatinin niedriger sein, als es die Nierenfunktion eigentlich erwarten ließe.
Unabhängig von einer Nierenerkrankung werden erhöhte Werte bei Dehydratation und Perfusionsstörung (prärenale Azotämie), Harnwegsobstruktion/-ruptur (postrenale Azotämie), bei sehr gut bemuskelten und trainierten Hunden sowie bei der Birma-Katze und bei fleischreicher Fütterung gesehen.
Von der IRIS (International Renal Interest Society) wird insbesondere Kreatinin zur Klassifizierung von Nierenerkrankungen herangezogen. Dabei ist vor allem die Einteilung der CNE in die Stadien 1 – 4 im Praxisalltag relevant. Im Stadium 1 (Frühstadium) liegt noch keine Azotämie vor. Stadium 2 wird durch eine geringgradige Azotämie definiert, hier sind oft keine oder nur milde klinische Symptome vorhanden. Stadium 3 zeichnet sich durch eine mittelgradige Azotämie und deutlicher werdende klinische Probleme aus. Stadium 4 wird oft auch als Endstadium bezeichnet, die Azotämie ist hochgradig.
SDMA
Symmetrisches Dimethylarginin (SDMA) ist ein Aminosäurederivat, das beim Proteinabbau frei wird. SDMA wird über das Glomerulum filtriert und so gut wie nicht rückresorbiert. Damit ist es ein weiterer Parameter für die GFR. Vorteil gegenüber dem Kreatinin ist, dass die SDMA-Konzentration weniger von der Muskelmasse abhängig und SDMA daher auch bei kachektischen Tieren aussagekräftig ist. SDMA ist im Rahmen der Früherkennung einer Nierenerkrankung nutzbar. Die Konzentration kann bereits bei sehr geringer GFR-Reduktion erhöht sein. Allerdings ist dies nicht konstant der Fall. Bei wenigen Patienten kann SDMA im Rahmen der biologischen Varianz sogar später als Kreatinin ansteigen. Es ist zu beachten, dass SDMA, wie auch Kreatinin, von Faktoren beeinflusst wird, die sich unabhängig vom Gesundheitszustand der Niere auf die GFR auswirken. Es steigt an bei Dehydratation und Minderperfusion der Niere (prärenale Azotämie) sowie bei Harnabflussstörung (postrenale Azotämie) und sinkt ab bei Hyperfiltration (Hyperthyreose, systemische Hypertension). Bei wachsenden Tieren und solchen mit erhöhtem Proteinumsatz ist es oft erhöht. Grundsätzlich sollten singulär angestiegene SDMA-Konzentrationen bei anderweitig unauffälligem Nierenprofil mehrfach kontrolliert werden. Nur bei dauerhafter Erhöhung kann von einer renalen Erkrankung ausgegangen werden.
SDMA wurde von der IRIS für die Stadieneinteilung der chronischen Nierenerkrankung mit aufgenommen.
| IRIS
Stages |
Kreatinin [μmol/l]
|
SDMA [μmol/l]
|
||
| Hund | Katze | Hund | Katze | |
| 1 | < 125 | < 140 | < 0,89 | < 0,89 |
| 2 | 125 – 250 | 140 – 250 | 0,89 – 1,73 | 0,89 – 1,24 |
| 3 | 251 – 440 | 251 – 440 | 1,78 – 2,67 | 1,29 – 1,88 |
| 4 | > 440 | > 440 | > 2,67 | > 1,88 |
Tab. 1: IRIS-Stadieneinteilung der CNE, adaptiert an den bei Laboklin verwendeten SDMA-Test (SI-Einheiten); Quelle: Laboklin
Cystatin C
Cystatin C wird zur Frühdiagnostik beim Menschen genutzt und von einigen Autoren für den Hund als der Kreatinin-Bestimmung überlegen angesehen. Allerdings hat eine neuere Studie die Sensitivität und Spezifität von Cystatin C als geringer gegenüber Kreatinin und SDMA beurteilt. Vorsicht scheint zudem bei Hunden mit D. mellitus oder Hyperadrenokortizismus geboten zu sein. Bei der CNE der Katze wurde eine relativ starke Überlappung der Werte zwischen gesunden und erkrankten Katzen gefunden. Dies macht Cystatin C bei Katzen zu einem unzuverlässigen Parameter.
Indoxylsulfat
Indoxylsulfat ist eines der wichtigsten urämischen Toxine. Es fällt aus dem Tryptophan-Stoffwechsel über den Abbau von Indol an. Das proteingebundene Toxin wird zu 90 % über Transporter im Tubulus in den Harn sezerniert und zu 10 % über das Glomerulum filtriert. Wird es aufgrund einer kombinierten Fehlfunktion von Glomerulum und Tubulus nicht adäquat ausgeschieden, führt es über die Induktion von oxidativem Stress zu weiteren Schäden und somit zur Progression der Nierenerkrankung. Auch ist ein negativer Einfluss auf den für die Nierenprogression wichtigen Phosphathaushalt wahrscheinlich.
Indoxylsulfat korreliert mit der GFR sowie mit den Konzentrationen von Harnstoff, Kreatinin und Phosphat im Serum bei Hunden und Katzen mit Nierenerkrankungen. Es steigt bereits in frühen Erkrankungsstadien (IRIS-Stadium 2) leicht an und ist am höchsten bei Tieren mit fortgeschrittener Nierenfunktionsstörung (IRIS-Stadium 4).
Da Indoxylsulfat ein urämisches Toxin ist, zeigt es nicht nur den Grad der GFR-Reduktion an, sondern sagt vielmehr auch etwas über den klinisch relevanten Zustand des Patienten aus. Indoxylsulfat kann somit eine konkrete Hilfe bei der Therapieentscheidung sowie der Einschätzung der Wirksamkeit durchgeführter therapeutischer Maßnahmen sein. Zudem ist es vielversprechend als wertvoller prognostischer Marker. Je höher der Wert, desto in- tensiver sollte an therapeutischen Maßnahmen zur Reduktion urämischer Toxine gearbeitet werden.
Die Blutentnahme sollte am gefasteten Tier erfolgen, da Indoxylsulfat nach einer proteinreichen Fütterung ansteigt. Für die Untersuchung wird Serum benötigt (abzentrifugiert + abpipettiert), das gekühlt versandt werden muss. Der Parameter wird über die relativ aufwändige HPLC-Methode bestimmt und aktuell nur von Laboklin angeboten.
Phosphat
Phosphat wird über die Niere ausgeschieden und ist damit ebenfalls ein Marker einer eingeschränkten Nierenfunktion. Allerdings sehen wir bei Patienten in früheren Stadien der CNE (IRIS 1+2) meist Phosphatkonzentrationen im Referenzbereich. Das liegt daran, dass bei Retention von Phosphat eine Gegenregulation eingeleitet wird. Diese wird vorrangig über Parathormon gesteuert und führt zu einer verminderten Rückresorption von Phosphat im Tubulus. So kann der Körper die Blut-Phosphat-Konzentration konstant halten. Dies funktioniert aber nur, wenn ausreichend Zeit vorhanden ist, diesen Kompensationsmechanismus zu aktivieren, und wenn die Menge an retiniertem Phosphat nicht das kompensierbare Maß überschreitet. In späteren Stadien der CNE (in der Regel ab IRIS-Stadium 3) kann die reduzierte Filtration von Phosphat nicht mehr durch eine geringere Rückresorptionsrate im Tubulus ausgeglichen werden. Erst dann steigt bei CNE der Phosphatwert über den Referenzbereich. Zu beachten ist, dass nicht nur das Phosphat selbst, sondern vor allem die Kompensationsmechanismen für die Progression der Nierenerkrankung verantwortlich gemacht werden. Deshalb wird empfohlen, den Phosphatwert unter einem bestimmten Zielbereich zu halten. Dieser Zielbereich unterscheidet sich vom Referenzwert. So empfiehlt die IRIS einen Phosphatwert zwischen 0,9 und 1,5 mmol/l (2,7 – 4,6 mg/dl) für Hunde und Katzen mit CNE (insbesondere in frühen IRIS-Stadien). Die angeratene Höchstgrenze für die Phosphatkonzentration liegt unter dem meist üblichen oberen Referenzwert.
Harnuntersuchung nicht vergessen
Ein einfacher, aber meist unterbewerter Nierenfunktionsparameter ist das Urin-spezifische Gewicht (USG). Bestimmt wird es mit einem Refraktometer. Das auf einigen Harn-Teststreifen ablesbare USG gibt für Tiere keine korrekten Werte wieder. Das USG ist ein Parameter zur Überprüfung der Funktion des Tubulus. Ist die Fähigkeit der Niere Harn zu konzentrieren gestört, bedeutet dies, dass der Tubulus seiner Funktion, Wasser zurück zu resorbieren, nicht ausreichend nachkommt. Ein reduziertes USG kann bereits vor dem Eintreten einer Azotämie auftreten. Typisch für eine Nierenerkrankung sind Werte zwischen 1008 und 1025 beim Hund bzw. 1008 und 1035 bei der Katze. Allerdings müssen andere Faktoren, die zu einem reduzierten USG führen können (z. B. bakterielle Infektionen, Hormonstörungen, Hyperkalzämie), ausgeschlossen werden.
Eine Proteinurie kann ebenfalls eine Nierenerkrankung anzeigen. Dies ist, ähnlich wie beim reduzierten USG, bereits vor Auftreten einer Azotämie möglich. Hierbei ist zu beachten, dass der Harn-Teststreifen für Katzen gerne sowohl falsch hohe als auch falsch niedrige Werte liefert. Ein zuverlässiges Ergebnis kann bei dieser Tierart nur mit Hilfe des Urin-Protein-Kreatinin-Quotienten (UP/C) erreicht werden. Die Bestimmung des UP/C sollte bei der Katze daher selbst dann erfolgen, wenn der Harn-Teststreifen kein Protein anzeigt. Für Hunde empfiehlt sich die Untersuchung des UP/C zur korrekten Quantifizierung der Proteinurie, sobald der Harn-Teststreifen ein positives Ergebnis liefert oder wenn das USG sehr niedrig ist (< 1012). Eine Proteinurie ist nur dann im Hinblick auf eine Nierenerkrankung aussagekräftig, wenn keine Entzündungsanzeichen im Harn vorhanden sind. Eine Sediment-Untersuchung sollte somit in jedem Fall parallel erfolgen. Weitere Faktoren, die zu einer (nicht-renalen) Proteinurie führen können, sind insbesondere: systemische Hypertension, Hyperthyreose, Hyperadrenokortizismus, Fieber und Hyperproteinämie.
Für die Verlaufsuntersuchung ist zu beachten, dass ein sinkender UP/C nur bei stabiler Nierenfunktion als Verbesserung zu bewerten ist. Verschlechtert sich die Nierenfunktion (zu erkennen an ansteigenden Kreatinin-Konzentrationen im Blut), stehen weniger Glomerula zur Verfügung, über die Protein verloren gehen kann. Der UP/C fällt möglicherweise ab, obwohl die Nierenerkrankung progressiv ist.
Fazit
Das klassische Nierenprofil besteht aus Biomarkern, die vorrangig die GFR widerspiegeln. Dabei eignet sich SDMA zur Früherkennung von Nierenerkrankungen.
Nicht zu unterschätzen ist der Wert der Harnuntersuchung. Das USG und der UP/CQuotient können bereits sehr früh Hinweise auf eine Nierenfunktionsstörung geben.
In späteren Stadien der CNE können Harnstoff und insbesondere Indoxylsulfat hilfreich bei der Einschätzung der Folgen der Erkrankung für den Patienten sein.
Dr. Jennifer von Luckner, Dr. Corinna Weber
Das Literaturverzeichnis erhalten Sie gerne auf Anfrage.