Vitamin E beim Sportpferd – ernährungsphysiologische Relevanz und Mangelpathologie
Vitamin E ist ein fettlöslicher Mikronährstoff und in der Pferdeernährung essenziell. Physiologisch relevant ist nahezu ausschließlich α-Tocopherol, wobei die natürliche Form RRR-α-Tocopherol aufgrund ihrer bevorzugten hepatischen Verarbeitung die höchste Bioverfügbarkeit besitzt.
Als lipidlösliches Antioxidans schützt Vitamin E Zellmembranen vor oxidativer Schädigung und ist für die neuromuskuläre Funktion von zentraler Bedeutung. Unter körperlicher Belastung steigt der Vitamin-E-Umsatz infolge vermehrter Bildung reaktiver Sauerstoffspezies an.
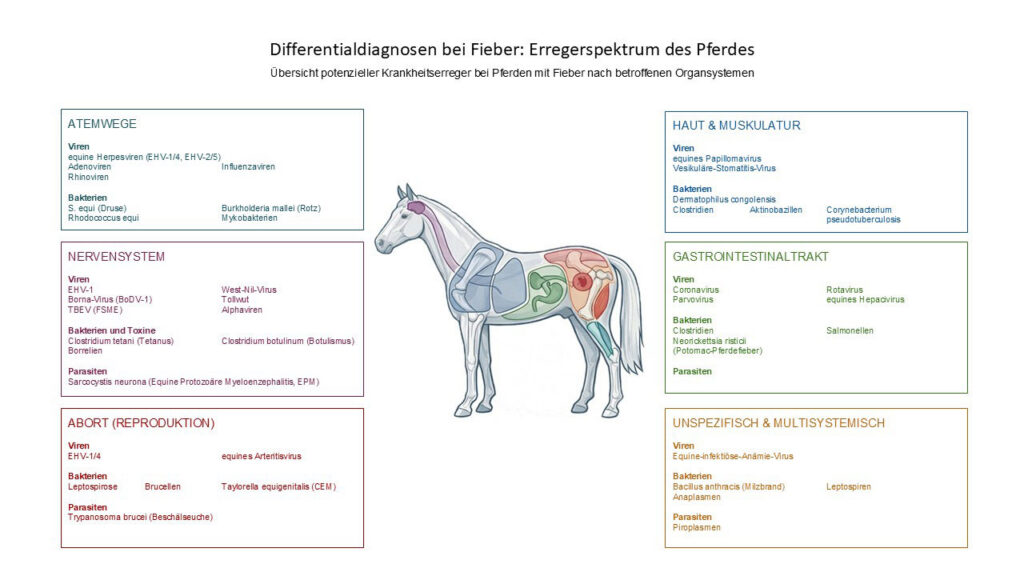
- Abb. 1: Differentialdiagnosen der häufigsten Erreger bei Pferden mit Fieber nach Organsystemen sortiert Bildquelle: Laboklin
Vitamin E wird ausschließlich von Pflanzen synthetisiert und ist in frischem Gras in hohen Konzentrationen vorhanden. Konservierte Futtermittel weisen durch Lagerungs- und Oxidationsprozesse deutlich reduzierte Gehalte auf, sodass Pferde ohne Weidegang ihren Bedarf nicht ausreichend decken können.
Der empfohlene tägliche Bedarf liegt bei 1–2 mg/kg Körpermasse, für Sportpferde bei mindestens 2 mg/kg KM. Bei erhöhter oxidativer Belastung oder muskulären Erkrankungen werden 4–6 mg/kg KM empfohlen.
Ein chronischer Vitamin-E-Mangel kann zu schwerwiegenden neuromuskulären Erkrankungen führen. Dazu zählen die Vitamin E deficient myopathy mit degenerativen Muskelveränderungen, die Equine Motor Neuron Disease (EMND) mit progressiver Degeneration motorischer Neurone sowie die Neuroaxonale Dystrophie/Equine Degenerative Myeloenzephalopathie (NAD/EDM), eine neuro-degenerative Erkrankung des jungen Pferdes, bei der Vitamin-E-Mangel als zentraler prädisponierender Faktor gilt.
Der Versorgungsstatus wird über die Serum-α-Tocopherol-Konzentration beurteilt; Werte >2,0 µg/ml gelten als adäquat.
Bei fehlender Grasaufnahme ist eine Supplementation obligat. Natürliches RRR-α-Tocopherol ist synthetischen Formen hinsichtlich der Bioverfügbarkeit überlegen. Eine über den Bedarf hinausgehende Supplementation zeigt bei gesunden Sportpferden jedoch keinen konsistenten Nutzen in Bezug auf Leistungsfähigkeit oder Marker des oxidativen Stresses.
Myopathien beim Islandpferd – labordiagnostische Einordnung und klinische Relevanz
Myopathien stellen beim Islandpferd eine zunehmend erkannte Ursache für Leistungsminderung und unspezifische Lahmheitsbilder dar. Aufgrund rassespezifischer biomechanischer Besonderheiten sowie subtiler klinischer Symptome werden muskuläre Erkrankungen häufig erst spät diagnostiziert. Eine kürzlich beschriebene chronisch idiopathische Myopathie scheint dabei eine Islandpferde-spezifische Entität darzustellen.
Betroffene Pferde zeigen überwiegend unspezifische klinische Symptome wie Leistungsabfall, diffuse Lahmheiten, Stolpern, erhöhte Atemfrequenz sowie eine verminderte Bereitschaft zur Ausführung bestimmter Gangarten. Akute klinische Zeichen einer klassischen Belastungsrhabdomyolyse fehlen in der Regel.
Die Serum-Creatinkinase (CK) stellt den wichtigsten labordiagnostischen Marker dar. Ruhewerte sind häufig normal oder nur geringgradig erhöht. Diagnostisch wegweisend ist ein belastungsabhängiger CK-Anstieg, der standardisiert nach 4 und 24 Stunden erfasst wird. Die CK-Spitzenwerte liegen typischerweise bei 2000–3000 U/L und damit deutlich unter den Werten von Pferden mit rezidivierender Belastungsmyopathie (Recurrent Exercise Rhabdomyolysis, RER).
Die CK-Kinetik besitzt eine höhere diagnostische Aussagekraft als Einzelmessungen. Reproduzierbare, moderate Anstiege nach Belastung sprechen für eine myopathische Genese, auch bei nur geringfügig erhöhten Absolutwerten. Ergänzend kann Aspartat-Aminotransferase (AST) zur Beurteilung länger bestehender Muskelschädigungen herangezogen werden. Entzündungsparameter sowie metabolische Routineprofile dienen primär dem Ausschluss systemischer oder entzündlicher Erkrankungen.
Die definitive Diagnosesicherung erfolgt mittels Muskelbiopsie aus dem Musculus semimembranosus. Histopathologisch zeigen sich chronische degenerative und regenerative Veränderungen mit zentralisierten Zellkernen, ohne Hinweise auf abnorme Glykogenablagerungen oder myofibrilläre Defekte.
Bei Islandpferden mit Leistungsminderung sollte die belastungsabhängige CK-Dynamik frühzeitig Bestandteil der Diagnostik sein. In Kombination mit der Muskelbiopsie ermöglicht sie eine valide Abgrenzung gegenüber anderen myopathischen und nicht-myopathischen Ursachen und stellt eine zentrale Grundlage für die klinische Entscheidungsfindung dar.
Fieber beim Pferd: Stellenwert der Labordiagnostik in der klinischen Entscheidungsfindung
Fieber stellt beim Pferd ein häufiges, jedoch unspezifisches klinisches Leitsymptom dar, dessen ätiologische Abklärung eine strukturierte diagnostische Vorgehensweise erfordert (Abb. 1). Ziel ist die frühzeitige Identifikation infektiöser oder systemischer Erkrankungen, die eine gezielte Therapie oder weiterführende Maßnahmen notwendig machen.
Nach Anamnese und klinischer Untersuchung kommt der Labordiagnostik eine zentrale Rolle zu. Hämatologische und klinisch-chemische Untersuchungen ermöglichen eine erste Einordnung des Entzündungsgeschehens sowie Hinweise auf mögliche Organbeteiligungen. Akute-Phase-Proteine besitzen hierbei eine besondere diagnostische Bedeutung. Serum Amyloid A (SAA) reagiert als Major-Akute-Phase-Protein des Pferdes rasch und hochsensitiv auf entzündliche Stimuli und eignet sich sowohl zur Detektion akuter Prozesse als auch zur Verlaufskontrolle. Fibrinogen zeigt eine verzögerte, länger anhaltende Erhöhung und ist insbesondere bei subakuten oder chronischen Entzündungen diagnostisch relevant. Aufgrund ihrer hohen Sensitivität, jedoch fehlenden Spezifität, müssen Akute-Phase-Proteine stets im klinischen Kontext interpretiert werden.
Zur ätiologischen Abklärung infektiöser Ursachen sind spezifische labordiagnostische Verfahren erforderlich. Molekulare Nachweismethoden, insbesondere PCR-basierte Verfahren in akkreditierten Laboren, gelten als Goldstandard für den direkten Erregernachweis. Sie zeichnen sich durch eine hohe analytische Sensitivität und Spezifität aus und ermöglichen eine gezielte Differenzierung relevanter bakterieller und viraler Pathogene. Point-of-Care-Tests können eine zeitnahe erste Orientierung bieten, ersetzen jedoch weder die umfassende Labordiagnostik noch die qualitätsgesicherte Befundinterpretation durch spezialisierte Labore.
In Abhängigkeit von den laborchemischen Ergebnissen und dem klinischen Verlauf können weiterführende diagnostische Maßnahmen, einschließlich bildgebender Verfahren oder gezielter Probenentnahmen, erforderlich sein. Insgesamt stellt die Labordiagnostik einen unverzichtbaren Bestandteil der Fieberabklärung beim Pferd dar und bildet die Grundlage für evidenzbasierte Therapieentscheidungen sowie für Maßnahmen zum Schutz des Bestandes.
Genetische Tests bei equinen Myopathien: evidenzbasierte Anwendung und genetische Grenzen
Die genetische Testung hat sich als diagnostisches Instrument bei equinen Myopathien etabliert, erfolgt jedoch bislang ohne verbindliche regulatorische Kontrolle. Daraus ergibt sich für Tierärztinnen und Tierärzte die Notwendigkeit, die Validität kommerziell angebotener Tests kritisch zu beurteilen. Ein genetischer Test sollte nur dann klinisch Anwendung finden, wenn die zugrunde liegende Variante nachweislich kausal mit der Erkrankung assoziiert ist und international anerkannte Validierungskriterien Beachtung finden.
Zu den grundlegenden Anforderungen an valide genetische Tests zählen eine geringe Allelfrequenz in der Allgemeinpopulation, eine hohe Übereinstimmung zwischen Genotyp und Phänotyp, ein funktionell relevanter Einfluss der Variante auf das kodierte Protein sowie eine Reproduzierbarkeit der Ergebnisse in peer-reviewten Studien. Diese Kriterien werden bislang nur von wenigen genetischen Tests für equine Myopathien erfüllt.
Derzeit existieren fünf bis sechs validierte genetische Tests für Muskelerkrankungen beim Pferd, darunter die Polysaccharid-Speicher-Myopathie Typ 1 (PSSM1; GYS1), die Myosin-Heavy-Chain-Myopathie (MYHM; MYH1), die hyperkaliämische periodische Paralyse (HYPP; SCN4A), die malig-ne Hyperthermie (MH; RYR1) sowie die Glykogen-Verzweigungsenzym-Defizienz (GBED; GBE1).
Die Identifikation der kausalen Varianten basierte jeweils auf streng phänotypisierten Fall-Kontroll-Studien unter Anwendung von Goldstandard-Diagnostik wie Muskelhistopathologie oder Elektromyographie. Die jeweiligen Mutationen zeigen eine hohe Krankheitsassoziation, eine niedrige Prävalenz in gesunden Populationen sowie einen klaren funktionellen Effekt auf das betroffene Protein.
Demgegenüber stehen kommerzielle genetische Testpanels für sogenannte Typ-2-Polysaccharid-Speicher-Myopathien (PSSM2), myofibrilläre Myopathien (MFM), Muscle Integrity Myopathy (MIM) und die rezidivierende Belastungsrhabdomyolyse (RER). Diese Tests basieren auf Varianten in Genen wie MYOT, FLNC, MYOZ3, PYROXD1, CACNA2D3 und COL6A3, deren pathogenetische Relevanz bislang nicht überzeugend belegt ist.
Mehrere unabhängige Studien konnten keine signifikante Assoziation zwischen diesen Varianten und histopathologisch bestätigten Myopathien nachweisen. Die Prävalenz der getesteten Varianten war bei erkrankten Pferden vergleichbar mit jener gesunder Kontrolltiere, was zu hohen Raten falsch-positiver und falsch-negativer Testergebnisse führte. Besonders auffällig ist die hohe Allelfrequenz dieser Varianten in der Allgemeinpopulation: Populations-genetische Analysen zeigen, dass bis zu 50 % der Warmblutpferde mindestens eine dieser Varianten tragen. Angesichts der deutlich niedrigeren Prävalenz klinisch manifester Muskelerkrankungen ist eine kausale Rolle dieser Varianten unwahrscheinlich; vielmehr handelt es sich vermutlich um benigne genetische Polymorphismen.
Auch für die genetische Diagnostik der rezidivierenden Belastungsrhabdomyolyse ist die Evidenz begrenzt. Die als ursächlich postulierte Px-Variante ist synonym und führt zu keiner Veränderung der Aminosäuresequenz. Ihre hohe Prävalenz in gesunden Thoroughbreds widerspricht einer kausalen pathogenetischen Bedeutung.
Zusammenfassend sollten genetische Tests bei equinen Myopathien ausschließlich dann eingesetzt werden, wenn sie streng validiert sind und mit Rasse, klinischem Erscheinungsbild sowie laborchemischen und histopathologischen Befunden übereinstimmen. Der unkritische Einsatz nicht validierter genetischer Testpanels birgt ein erhebliches Risiko für Fehldiagnosen und unangemessene züchterische Selektion.
Entwicklung neuer diagnostischer Tests für infektiöse Endometritis bei der Stute
Die infektiöse Endometritis stellt eine der häufigsten Ursachen für Subfertilität und Infertilität bei der Stute dar. Sie tritt entweder als persistierende entzündliche Reaktion nach der Bedeckung oder als chronische bakterielle Infektion auf. Während die Mehrzahl der Stuten uterine bakterielle Kontaminationen innerhalb von 6–24 h effektiv eliminiert, entwickeln etwa 10–15 % eine chronische Endometritis, die eine erfolgreiche Trächtigkeit verhindert.
Die klassische Diagnostik der infektiösen Endometritis basiert auf bakteriologischer Kultur, zytologischer Untersuchung sowie molekularbiologischen Verfahren wie der PCR. Diese Methoden erfassen jedoch primär planktonisch vorliegende, metabolisch aktive Bakterien. Rezidivierende Infektionen können dennoch auftreten, da Erreger entweder in anatomischen Reservoiren (z. B. Klitorisfossa), in einem metabolisch inaktiven (dormanten) Zustand tief im Endometrium oder als bakterielle Biofilme persistieren. Diese Formen entziehen sich häufig sowohl der konventionellen Diagnostik als auch der antibiotischen Therapie.
Zur Detektion dormant persistierender Keime wurde ein diagnostisch-therapeutisches Aktivierungskonzept entwickelt, bei dem ruhende Bakterien im Endometrium stimuliert werden, sodass sie anschließend mittels konventioneller Kultur oder PCR nachweisbar und therapeutisch zugänglich werden. Dieses Vorgehen stellt einen wesentlichen Fortschritt in der Diagnostik subklinischer und rezidivierender Endometritiden dar.
Ein bislang ungelöstes diagnostisches Problem ist der zuverlässige in-vivo-Nachweis bakterieller Biofilme im Uterus. Biofilme schützen Bakterien effektiv vor der Immunabwehr und antimikrobiellen Substanzen und fördern die Entwicklung antimikrobieller Resistenzen. Zwar ist experimentell belegt, dass typische Erreger der equinen Endometritis wie Streptococcus equi ssp. zooepidemicus, Escherichia coli oder Pseudomonas aeruginosa Biofilme bilden können, jedoch existiert derzeit keine etablierte klinische Diagnostikmethode für uterine Biofilme.
Aktuelle Forschungsansätze fokussieren sich daher auf den Nachweis spezifischer Bestandteile der Biofilm-Matrix in niedrigvolumigen uterinen Lavagen. Diese Matrix besteht aus Proteinen, Lipiden, Polysacchariden und Nukleinsäuren. Proteomische und lipidomische Analysen konnten bereits Unterschiede zwischen planktonischen und biofilmbildenden Bakterien identifizieren, darunter biofilmspezifische Proteine und Membranlipide mit potenzieller diagnostischer Relevanz. Ziel ist die Entwicklung eines robusten, klinisch einsetzbaren Tests, der eine gezielte Diagnose und damit eine differenzierte, biofilmspezifische Therapie ermöglicht.
Zusammenfassend sollten bei rezidivierender infektiöser Endometritis neben frei vorliegenden Bakterien auch dormant persistierende Keime und bakterielle Biofilme in die diagnostische Überlegung einbezogen werden. Die Entwicklung biofilmspezifischer diagnostischer Verfahren stellt einen entscheidenden Schritt dar, um die Therapie zu optimieren und den Einsatz von Antibiotika gezielter und verantwortungsvoller zu gestalten.
Eine Auswahl unserer Leistungen zu den o. g. Themen:
- Bestimmung von Einzelvitaminen und Vitaminprofile (groß und klein)
- Muskel-Screening einfach und erweitert
- verschiedene PCR-Profile zum Erregernachweis nach Organsystem (z. B. Atemwege I-IV)
- zahlreiche Gentests (z. B. Polysaccharid-Speicher-Myopathie Typ 1, PSSM; Immune mediated myositis & MYH1 myopathy, MYHM; Hyperkaliämische periodische Paralyse, HYPP; Equine maligne Hyperthermie, EMH; Glycogen branching enzyme deficiency, GBED)
- Zuchthygiene
Jana Pohl